近年来,由于一次性技术的工艺灵活、低交叉污染风险及显著节省清洁/清洗时间等优势,一次性技术在生物制药领域已被广泛应用。而如何识别、降低、控制一次性使用系统在其生命周期内的质量风险,成为了生物制药行业的新挑战。
并且,根据《药品GMP指南第二版》(2023版)中《GMP无菌制剂》上册的第18.1章内容,对一次性使用技术的应用做出了如下建议:
◇18.1.1章节 “一次性使用技术的应用”:
(5)一次性使用技术泄漏的预防和处理
泄漏预防措施包括以下内容...
...一次性使用技术耗材在使用前应进行完整
性测试,避免使用有完整性缺陷的耗材...
(6)一次性使用技术使用中的注意问题
...企业在使用一次性使用技术前,建议确认其
完整性,或使用后确认...
由此可见,药品生产过程中对一次性技术的完整性确认测试是降低潜在风险点的关键环节,目前也已被纳入技术指南。
为此,科百特专为生物制药用户应对一次性使用系统质量挑战而研发新品——Certitest ® Bag完整性测试仪,旨在低成本、低门槛、高效率地帮助用户在生产过程中对一次性生物工艺袋实施完整性检测。

检测原理
Certitest ® Bag完整性测试仪基于压力衰减原理,运行时,根据配方参数,持续充气加压至预设压力值,并通过稳压步骤释放一次性生物工艺袋的部分弹性形变后,将气源从测试部位隔离,采集在预设时间段内的压力变化,从而判断是否存在泄漏。相较于概率性的泄漏检测技术,如微生物挑战和液下气泡试验法,压力衰减检测法具备对袋体无损且确定性的特性。
应用领域
Certitest ® Bag完整性测试仪可用于全尺寸2D/3D 一次性生物工艺袋的使用前或使用后完整性检测。
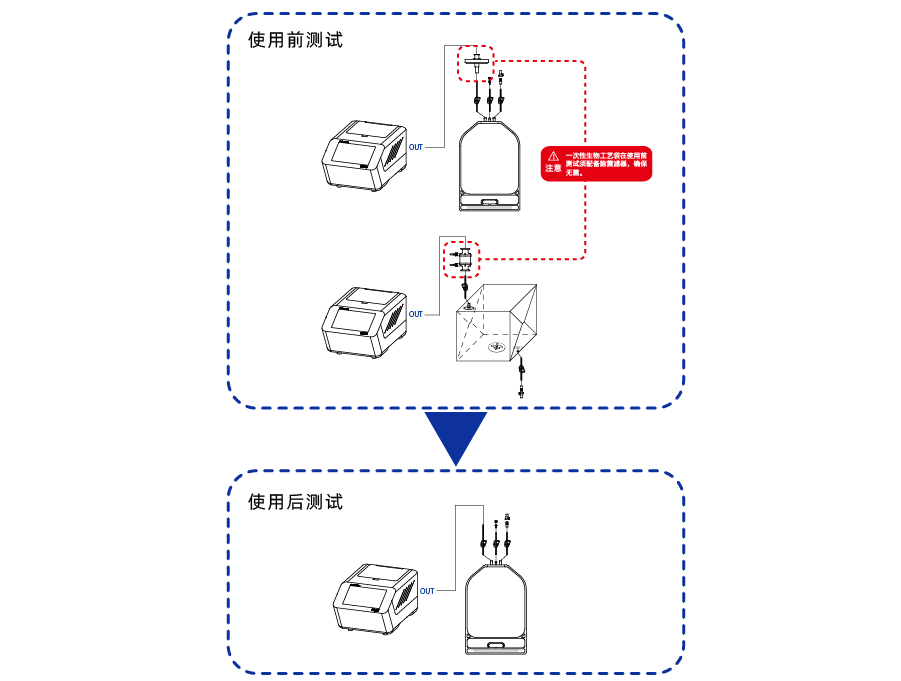
产品特点
Certitest ® Bag完整性测试仪支持在不高于300 mbar的压力下自定义测试压力值。仪器可二段式充气控制,快速充气,精确控压。且支持自定义稳压时长和测试时长,适配各种测试场景。
同时,仪器配备高精度传感器,压降曲线实时显示。完成配方参数编辑后,即可一键调用,可使用扫码枪快速读取一次性生物工艺袋信息,确保用户无忧使用。
满足数据完整性合规要求
- 拥有完整的审计追踪功能,满足FDA 21 CFR Part 11要求,轻松溯源,操作留痕;
- 支持数据以及日志的PDF文件导出,一键备份/还原;
- 支持多级权限分配,自定义用户组权限;
- 全局应用的多层级密码策略,满足计算机化系统软件验证要求。
强大的硬件支持
- 仪器标配16G超大内存,无惧卡顿;
- 128G固态硬盘,支持10000条以上数据/日志存储;
- 一体化阀组设计,密封性高,系统稳定不易泄漏;
- 快速进/出气接头,即插即用。
仪器参数
订购信息
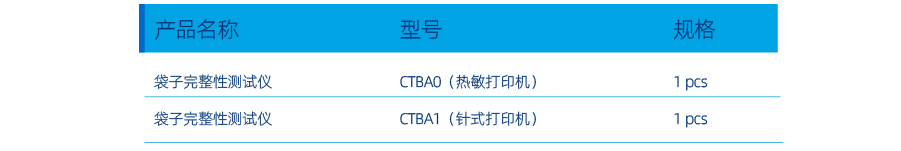
一次性产品在生物制药研发生产上的重要性日趋显著,科百特作为国内优质过滤分离全产业链供应商,始终坚持以客户需求为导向,以创新技术为驱动,不断开发优质产品,提供更便捷、高效、可靠支持。





